Contenido
Aunque todos los átomos del mismo elemento contienen el mismo número de protones, el número de neutrones puede variar. Saber cuántos neutrones tiene un átomo en particular puede ayudarlo a determinar si la partícula es regular en ese elemento o un isótopo, que tendrá más o menos neutrones. Determinar el número de neutrones en un átomo es bastante simple y no requiere ningún experimento. Para calcular el número de neutrones en un átomo o isótopo regular, siga estas instrucciones con una tabla periódica en la mano.
Pasos
Método 1 de 2: encontrar el número de neutrales en un átomo común
Localiza el elemento en la tabla periódica. Para este ejemplo, veamos el SO (OS), que está en la sexta fila, de arriba a abajo.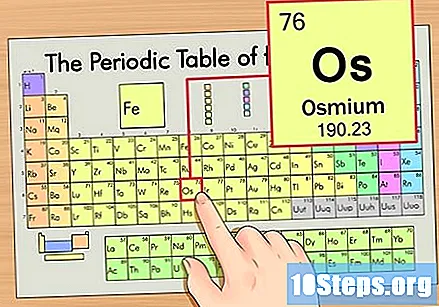
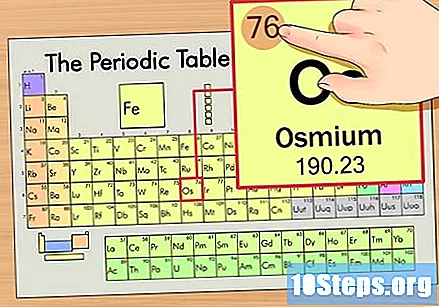
Encuentra el número atómico del elemento. Este suele ser el número más visible para un elemento en particular y suele estar encima de su símbolo (en la tabla que estamos usando, de hecho, no hay ningún otro número en la lista). El número atómico es el número de protones en un solo átomo de ese elemento.. El número de Os es 76, lo que significa que un átomo de osmio tiene 76 protones.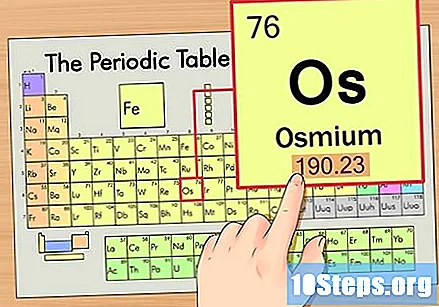
Encuentra el peso atómico del elemento. Este número generalmente se encuentra debajo del símbolo atómico. Tenga en cuenta que la tabla de este ejemplo se basa únicamente en el número atómico y no enumera el peso atómico. Este no siempre será el caso. El osmio tiene un peso atómico de 190,23.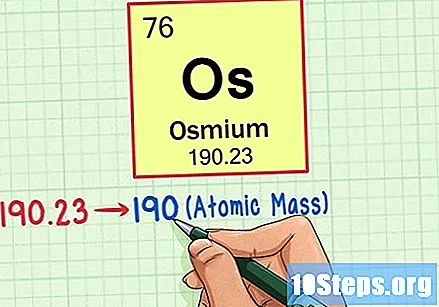
Redondea el peso atómico al número entero más cercano para encontrar la masa atómica. En nuestro ejemplo, 190,23 se redondearía a 190, lo que daría como resultado una masa atómica de 190 para el osmio.- La masa atómica es un promedio de los isótopos del elemento. Por tanto, no suele ser un número entero.
Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se encuentra en sus protones y neutros, restar el número de protones (es decir, el número atómico) de la masa atómica le dará el número calculado de neutrones en el átomo. El número después del punto decimal generalmente representa una masa muy pequeña de electrones en el átomo. En nuestro ejemplo, esto es: 190 (masa atómica) - 76 (número de protones) = 114 (número de neutrones).
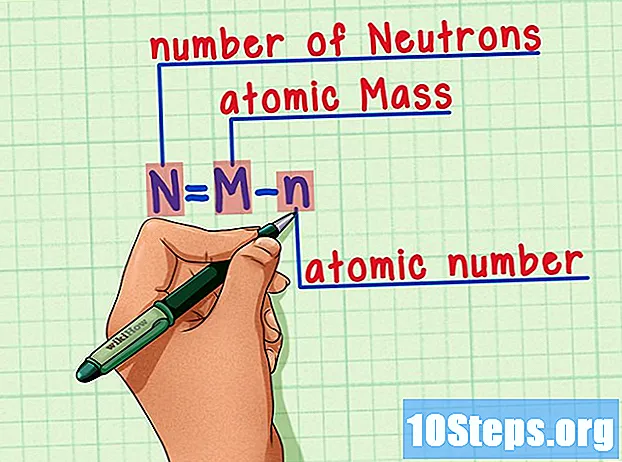
Recuerda la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula: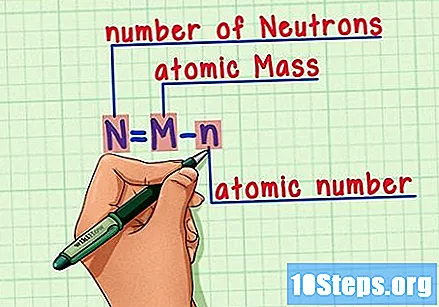
- N = M - n.
- N = número de norteeutrones.
- M = METROtueste atómico.
- n = nortehúmero atómico.
- N = M - n.
Método 2 de 2: encontrar el número de neutrones en un isótopo
Localiza el elemento en la tabla periódica. Por ejemplo, usemos el isótopo de carbono 14. Dado que la forma no isotópica del carbono-14 es simplemente carbono (C), busque este elemento en la tabla periódica (en la segunda fila).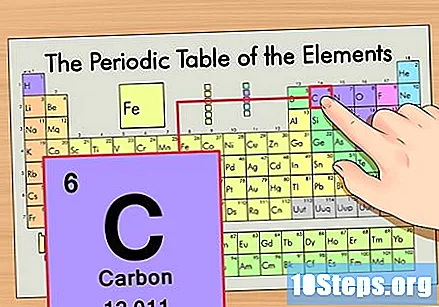
Encuentra el número atómico del elemento. Este suele ser el número más visible para un elemento en particular y suele estar encima de su símbolo (en la tabla que estamos usando, de hecho, no hay ningún otro número en la lista). El número atómico es el número de protones en un solo átomo de ese elemento.. C es el número 6, lo que significa que un átomo de carbono tiene 6 protones.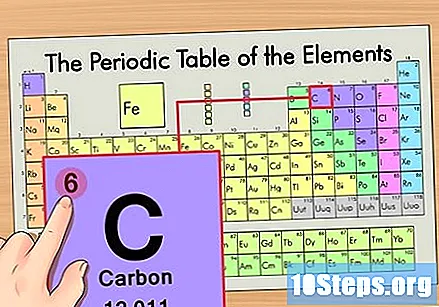
Encuentra la masa atómica. Esto es increíblemente fácil con los isótopos, ya que reciben el nombre de su masa atómica. El carbono 14 tiene una masa atómica de 14. Una vez que encuentra la masa atómica del isótopo, el proceso para encontrar el número de neutrones es el mismo que se usa para los átomos ordinarios.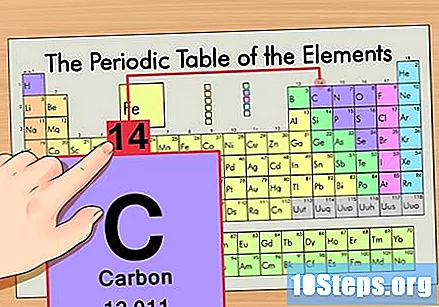
Reste el número atómico de la masa atómica. Dado que la gran mayoría de la masa de un átomo se encuentra en sus protones y neutros, restar el número de protones (es decir, el número atómico) de la masa atómica le dará el número calculado de neutrones en el átomo. El número después del punto decimal generalmente representa una masa muy pequeña de electrones en el átomo. En nuestro ejemplo, esto es: 14 (masa atómica) - 6 (número de protones) = 8 (número de neutrones).
Recuerda la fórmula. Para encontrar la cantidad de neutrones en el futuro, simplemente use esta fórmula: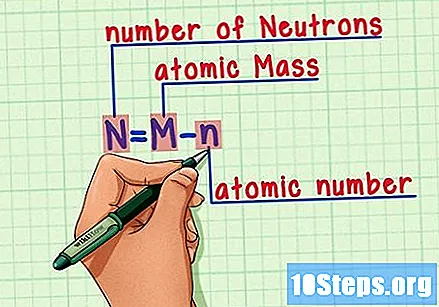
- N = M - n.
- N = número de norteeutrones.
- M = METROtueste atómico.
- n = nortehúmero atómico.
- N = M - n.
Consejos
- El osmio, un metal sólido a temperatura ambiente, deriva su nombre de la palabra griega que significa "olor", "osme".
- Los protones y neutrones constituyen casi todo el peso de los elementos, mientras que los electrones y otras partículas diversas representan una masa despreciable (que se aproxima a la masa cero). Dado que un protón tiene aproximadamente el mismo peso que un neutro y el número atómico representa el número de protones, simplemente podemos restar el número de protones de la masa total.
- Si no está seguro de qué número es cuál en la tabla periódica, recuerde que generalmente se compone del número atómico (es decir, el número de protones), que comienza con 1 (hidrógeno) y sube una unidad por de izquierda a derecha, terminando en 118 (Ununóctio). Esto se debe a que la cantidad de protones en un átomo determina cuál es ese átomo, lo que facilita la organización de la característica elemental (por ejemplo, un átomo con 2 protones siempre será helio, al igual que otro átomo con 79 protones siempre será oro).