Contenido
El porcentaje de masa determina el porcentaje de cada elemento que forma un compuesto químico. Para encontrar este valor, necesitará la masa molar de los elementos compuestos en gramos / moles o la cantidad de gramos utilizados para crear la solución. El porcentaje de masa se puede calcular de forma sencilla mediante una fórmula básica que divide la masa del elemento (o soluto) por la masa del compuesto (o solución).
Pasos
Método 1 de 2: Encontrar el porcentaje de masa con masas dadas
- Defina la ecuación para el porcentaje de masa de un compuesto. La fórmula básica de un compuesto es: porcentaje de masa = () x 100. Debes multiplicar el resultado por 100 al final para expresar los valores como porcentajes.
- La masa de un compuesto químico que le interesa es la masa dada en el problema. Si no se proporciona este valor, consulte el siguiente método y aprenda a encontrar el porcentaje de masa cuando no se proporciona la masa.
- La masa total de un compuesto se calcula sumando las masas de todos los elementos utilizados para crear el compuesto o la solución.
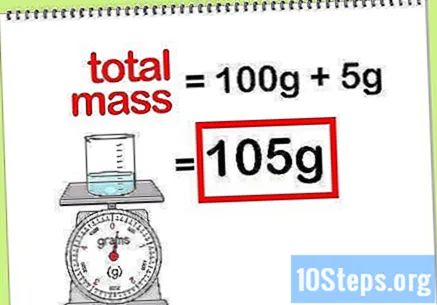
Calcula la masa total del compuesto. Cuando conoce el valor de masa de todos los elementos o compuestos que se agregan, simplemente debe sumarlos para calcular la masa del compuesto o la solución final. Este valor será el denominador en el cálculo del porcentaje de masa.- Por ejemplo: ¿Cuál es el porcentaje de masa de 5 g de hidróxido de sodio disueltos en 100 g de agua?
- La masa total del compuesto es la cantidad de peróxido de sodio más la cantidad de agua: 100 g + 5 g, totalizando una masa de 105 g.

Identifica la masa del químico en cuestión. Cuando necesitas encontrar el porcentaje de masa, el problema quiere que encuentre la masa de un elemento específico (el elemento en cuestión) como un porcentaje de la masa total de todos los elementos. Tenga en cuenta la masa del elemento en cuestión. Este valor será el numerador en el cálculo del porcentaje de masa.- Por ejemplo, la masa del elemento es 5 g de hidróxido de sodio.
- Sustituye las variables en la fórmula de porcentaje de masa. Después de determinar los valores para cada variable, reemplácelos en la ecuación.
- Por ejemplo: porcentaje de masa = () x 100 = () x 100.

Calcula el porcentaje de masa. Ahora que la ecuación está formada, simplemente resuélvala para calcular el porcentaje de masa. Divida la masa del elemento por la masa total del compuesto y multiplique por 100. El resultado será el porcentaje de masa del elemento químico.- Por ejemplo: () x 100 = 0.04761 x 100 = 4.751%. Por tanto, el porcentaje en masa de 5 g de hidróxido de sodio disuelto en 100 g de agua es del 4,751%.
Método 2 de 2: Encontrar el porcentaje de masa con masas no dadas
- Defina la ecuación para el porcentaje de masa de un compuesto. La fórmula básica para el porcentaje de masa de un compuesto es: porcentaje de masa = () x 100. Debes multiplicar el resultado por 100 al final para expresar los valores como porcentajes.
- Cuando no conozca los valores de masa, puede encontrar el porcentaje de masa de un elemento del compuesto usando la masa molar.
- Por ejemplo: ¿Cuál es el porcentaje de masa de hidrógeno en una molécula de agua?.
Escribe el fórmula química. Si no se proporcionan las fórmulas químicas de cada compuesto, deberá escribirlas. De lo contrario, vaya al paso "Hallar la masa de cada elemento".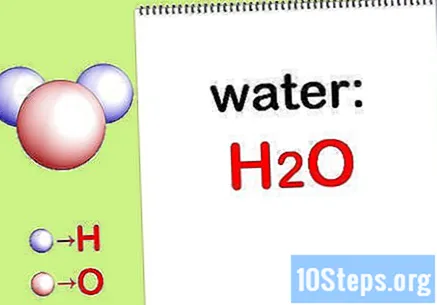
- Por ejemplo, escribe la fórmula química del agua: H2LA.
Encuentra la masa de cada elemento en el compuesto. Busque el peso molecular de cada elemento de las fórmulas químicas consultando la tabla periódica. Generalmente, la masa de un elemento se puede encontrar debajo del símbolo del elemento químico. Tenga en cuenta las masas de cada elemento del compuesto.
- Por ejemplo, la masa molecular del oxígeno es 15.9994 y la del hidrógeno es 1.0079.
Multiplica las masas por la relación molar. Identifica cuántos moles de cada elemento hay en el compuesto químico. El número de moles viene dado por el número suscrito del compuesto. Multiplica la masa molecular de cada elemento por la relación molar.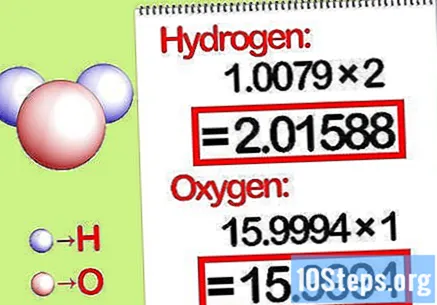
- Por ejemplo, la relación molar de hidrógeno a oxígeno en agua es 2: 1. Por lo tanto, multiplique el peso molecular del hidrógeno por dos (1.00794 X 2 = 2.01588) y deje el peso molecular del oxígeno como está (15.9994).
Calcula la masa total del compuesto. Suma la masa total de todos los elementos del compuesto. Usando las masas calculadas por la relación molar, es posible calcular la masa total del compuesto. Este número será el denominador de la ecuación de masa porcentual.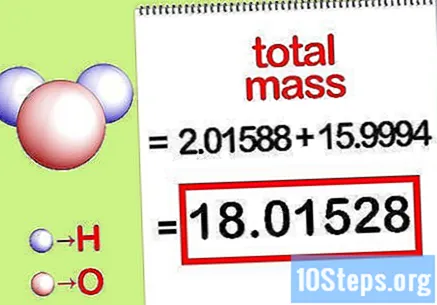
- Por ejemplo, agregue 2.01588 g / mol (la masa de dos moles de átomos de hidrógeno) con 15.9994 g / mol (la masa de un solo mol de un átomo de oxígeno) y obtenga 18.01528 g / mol.
Identifica la masa del elemento en cuestión. Cuando necesitas encontrar el porcentaje de masa, el problema quiere que encuentre la masa de un elemento específico en un compuesto como un porcentaje de la masa total de todos los elementos. Identifica la masa del elemento en cuestión y escríbela. Es el valor de masa calculado utilizando la relación molar. Este valor es el numerador de la ecuación de porcentaje de masa.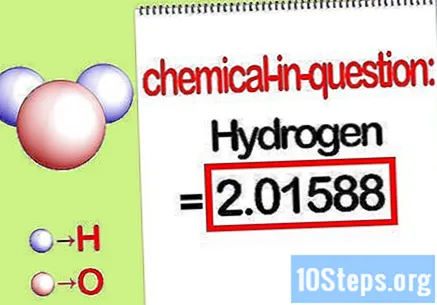
- Por ejemplo, la masa de hidrógeno del compuesto es 2.01588 g / mol (la masa de dos moles de átomos de hidrógeno).
- Sustituye las variables en la fórmula de porcentaje de masa. Después de determinar los valores para cada variable, reemplácelos en la ecuación definida en el primer paso: porcentaje de masa = () x 100.
- Por ejemplo: porcentaje de masa = () x 100 = () x 100.
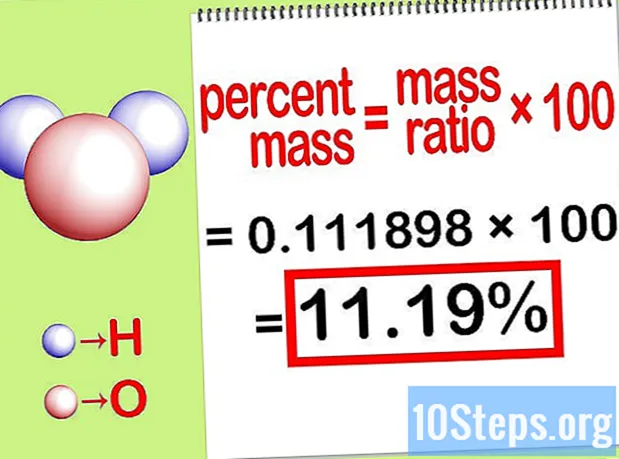
Calcula el porcentaje de masa. Ahora que la ecuación está formada, simplemente resuélvala para calcular el porcentaje de masa. Divida la masa del elemento por la masa total del compuesto y multiplique por 100. El resultado será el porcentaje de masa del elemento químico.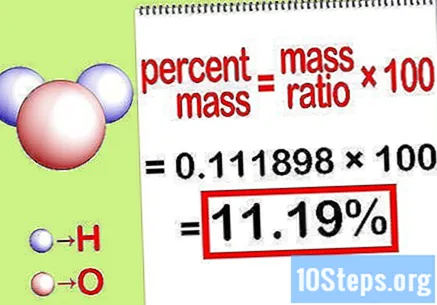
- Por ejemplo, porcentaje de masa = () x 100 = 0,111189 x 100 = 11,18%. Por tanto, el porcentaje de masa de átomos de hidrógeno en una molécula de agua es del 11,18%.